Navigare tra gli standard della farmacopea globale e la qualità dell'acqua per le utenze critiche

Il rispetto dei rigorosi standard della farmacopea è fondamentale per garantire la qualità, la sicurezza e la conformità alle normative dei prodotti farmaceutici. Poiché i leader nello sviluppo e nella produzione di farmaci stabiliscono il ritmo del settore, non si può sopravvalutare l'importanza della qualità dell'acqua per le utility critiche nel rispetto di questi standard.
Comprendere gli standard della Farmacopea: Una base per l'assicurazione della qualità
Le farmacopee, istituite da autorità regionali o nazionali, fungono da depositi completi di standard e specifiche di qualità per i farmaci all'interno di una specifica giurisdizione. Questi standard comprendono parametri cruciali come indicazioni, dosaggi e misure di controllo della qualità, costituendo il quadro normativo che regola la produzione farmaceutica.
Specifiche della Farmacopea per Stati Uniti, Europa e Asia
Una farmacopea è una raccolta legalmente vincolante di standard e specifiche di qualità preparata da un'autorità regionale o nazionale per i farmaci utilizzati in una specifica regione o paese. Queste specifiche sono fondamentali per le indicazioni, i dosaggi e altri fattori essenziali per garantire il controllo normativo dei farmaci. L'obiettivo principale delle farmacopee internazionali è quello di stabilire uno standard mondiale di qualità e specifiche d'uso uniformi.
Norme USP, EP e JP Pharmacopeia
I Paesi sviluppano farmacopee nazionali per sostenere la salute generale delle loro popolazioni attraverso standard e specifiche coerenti dei farmaci. Tre delle organizzazioni più riconosciute a livello mondiale sono la Farmacopea degli Stati Uniti (USP), la Farmacopea Europea (EP) e la Farmacopea Giapponese (JP).
Farmacopea degli Stati Uniti (USP): In qualità di principale organizzazione indipendente e senza scopo di lucro, l'USP stabilisce lo standard di riferimento per la qualità, la forza e la purezza dei farmaci a livello globale. Le aziende farmaceutiche di tutto il mondo si affidano alle monografie USP per garantire la conformità ai rigorosi parametri di garanzia della qualità imposti da enti normativi come la Food and Drug Administration (USFDA) degli Stati Uniti.
Farmacopea europea (EP): La EP fornisce una raccolta completa di monografie legalmente vincolanti che definiscono gli standard per gli ingredienti, le forme di dosaggio e i metodi di analisi per l'industria farmaceutica europea. La conformità alle specifiche della EP è essenziale per accedere al mercato europeo e garantire l'accettazione del prodotto.
Farmacopea giapponese (JP): La JP, che risale al 1886, stabilisce criteri, specifiche e metodi di prova standard per garantire la qualità e la sicurezza dei farmaci in Giappone. I produttori farmaceutici di tutto il mondo collaborano strettamente con il segretariato della JP per garantire l'allineamento con i più recenti progressi scientifici, medici e tecnologici.
Farmacopea cinese (CP): Emergendo come attore significativo nel panorama farmaceutico globale, la CP stabilisce standard e specifiche per i farmaci in Cina. Con la crescente influenza della Cina nell'industria farmaceutica, l'adesione alle linee guida della CP sta diventando sempre più importante per le aziende che vogliono accedere al mercato cinese e garantire la qualità dei prodotti.
Linee guida della Farmacopea per l'acqua pura
Le aziende farmaceutiche utilizzano ingredienti farmaceutici attivi (API) per produrre farmaci. Questi ingredienti sono gli elementi che producono l'effetto desiderato, sia esso la prevenzione, il trattamento, la cura o la diagnosi di una specifica condizione o malattia. I farmaci combinati contengono più di un ingrediente attivo che può agire in modo diverso per trattare vari sintomi.
Le linee guida della Farmacopea sono fondamentali per garantire che tutti gli API agiscano allo stesso modo tra i diversi marchi, compresi i farmaci generici. Le aziende che utilizzano gli API per fabbricare prodotti devono impiegare processi rigorosi per promuovere l'alta qualità e la conformità. Una delle parti più importanti di questi processi è l'utilizzo del tipo corretto di acqua purificata per una specifica fase di produzione.
MECO fornisce alle aziende farmaceutiche i sistemi MASTERpak™ che offrono una soluzione di purificazione efficiente e facile da usare. Progettiamo questi sistemi con tecnologie avanzate per garantire la produzione di acqua di alta qualità conforme alle linee guida della farmacopea.
Qualità dell'acqua per le utenze critiche:
Garantire la conformità agli standard della Farmacopea
Nella produzione farmaceutica, l'acqua è un ingrediente fondamentale per vari processi, tra cui la formulazione, la pulizia e il controllo qualità. La qualità dell'acqua utilizzata in questi servizi critici, tra cui l'acqua per iniezione (WFI), l'acqua purificata e l'acqua ultrapura, influisce direttamente sulla qualità del prodotto e sulla conformità agli standard della farmacopea.
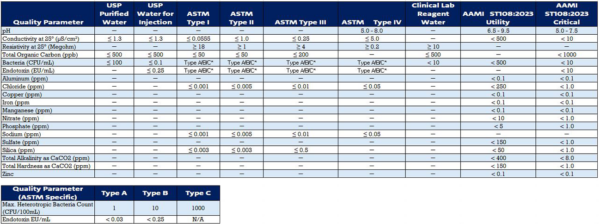
 Acqua per iniezione (WFI)
Acqua per iniezione (WFI)
L'acqua per uso iniettabile è l'acqua di più alta qualità utilizzata nella produzione farmaceutica e soddisfa i rigorosi standard di purezza e sterilità della farmacopea. È essenziale per la ricostituzione dei farmaci, la diluizione delle formulazioni e altri processi critici in cui la purezza dell'acqua è fondamentale.
Farmacopea degli Stati Uniti (USP):
- Conducibilità:
- Non più di 1,3 µS/cm a 25°C
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico (Nsu-Compendiale)
- Test di enumerazione: Non più di 10 UFC/100 mL
Farmacopea europea (EP):
- Conducibilità:
- Non più di 1,3 µS/cm a 20°C
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico (Non conforme)
- Test di enumerazione: Non più di 10 UFC/100 mL
Farmacopea giapponese (JP):
- Conducibilità:
- Non più di 2,1 µS/cm
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico
- Test di enumerazione: Non più di 10 UFC/100 mL
Farmacopea cinese (CP):
- Conducibilità:
- Non più di 1,3 µS/cm
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico
- Test di enumerazione: Non più di 10 UFC/100 mL
Questi standard garantiscono che l'acqua per iniezione (WFI) soddisfi i criteri di purezza e qualità richiesti per l'uso nei processi di produzione farmaceutica. Le aziende farmaceutiche devono attenersi a questi standard per mantenere l'integrità del prodotto e rispettare i requisiti normativi nelle rispettive regioni.
Acqua purificata (PW)
L'acqua purificata soddisfa le specifiche della farmacopea per quanto riguarda la purezza chimica e microbiologica ed è utilizzata in vari processi farmaceutici, tra cui la formulazione, la pulizia e i test di laboratorio. È fondamentale per mantenere l'integrità del prodotto e garantire la conformità ai requisiti normativi.
Farmacopea degli Stati Uniti (USP):
- Conducibilità:
- Non più di 1,3 µS/cm a 25°C
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico
- Test di enumerazione: Non più di 100 UFC/mL
Farmacopea europea (EP):
- Conducibilità:
- Non più di 5,1 µS/cm a 20°C
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico
- Test di enumerazione: Non più di 100 UFC/mL
Farmacopea giapponese (JP):
- Conducibilità:
- Non più di 4,3 µS/cm a 25°C
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico
- Test di enumerazione: Non più di 100 UFC/mL
Farmacopea cinese (CP):
- Conducibilità:
- Non più di 5,1 µS/cm a 25°C
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico
- Test di enumerazione: Non più di 100 UFC/mL
Questi standard garantiscono che l'acqua purificata soddisfi i criteri di purezza e qualità richiesti per i processi di produzione farmaceutica. È essenziale che le aziende farmaceutiche aderiscano a questi standard per mantenere l'integrità del prodotto e rispettare i requisiti normativi nelle rispettive regioni.
Acqua ultrapura (UPW)
L'acqua ultrapura supera gli standard della farmacopea per quanto riguarda la purezza dell'acqua e viene utilizzata in applicazioni farmaceutiche sensibili, come la cromatografia, la biologia molecolare e i test analitici. Il suo livello di purezza ultraelevato garantisce precisione e affidabilità nelle procedure di laboratorio critiche.
Farmacopea degli Stati Uniti (USP):
- Conducibilità:
- Non più di 1,3 µS/cm a 25°C
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico
- Test di enumerazione: Non più di 100 UFC/mL
Farmacopea europea (EP):
- Conducibilità:
- Non più di 0,1 µS/cm a 25°C
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico
- Test di enumerazione: Non più di 10 UFC/mL
Farmacopea giapponese (JP):
- Conducibilità:
- Non più di 0,1 µS/cm a 25°C
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico
- Test di enumerazione: Non più di 100 UFC/mL
Farmacopea cinese (CP):
- Conducibilità:
- Non più di 0,1 µS/cm a 25°C
- Totale
- Carbonio organico (TOC): Non più di 500 ppb
- Batterico
- Endotossine: non più di 0,25 EU/mL
- Microbico
- Test di enumerazione: Non più di 100 UFC/mL
Questi standard garantiscono che l'acqua ultrapura soddisfi i rigorosi requisiti di qualità specificati dalle norme farmacopeiche, rendendola adatta all'uso in applicazioni farmaceutiche sensibili, test analitici e ricerca. Le aziende farmaceutiche devono attenersi a questi standard per mantenere l'integrità del prodotto e rispettare i requisiti normativi nelle rispettive regioni.
Collaborare con MECO per soluzioni complete di depurazione dell'acqua
In MECO, il nostro approccio completo alle soluzioni di purificazione dell'acqua è studiato appositamente per le aziende biotecnologiche, farmaceutiche, di scienze biologiche e di ricerca e sviluppo. Progettiamo e produciamo tutte le tecnologie necessarie per produrre acqua per iniezione (WFI), acqua purificata, acqua ultrapura e vapore puro, garantendo ai nostri clienti l'accesso a una gamma completa di soluzioni di purificazione dell'acqua leader del settore.
Guidare l'innovazione e l'eccellenza
Con quasi un secolo di esperienza nell'industria dell'acqua, MECO si è affermata come fornitore leader di soluzioni per la purificazione dell'acqua. Dal 1928, forniamo sistemi all'avanguardia, progettati per soddisfare i severi requisiti delle linee guida della farmacopea.
MECO è orgogliosa dei suoi impianti di produzione a Mandeville, LA, e San Diego, CA (Water Works), dove progetta e produce tutte le tecnologie necessarie per produrre acqua per iniezione (WFI), acqua purificata (PW), acqua ultrapura (UPW) e vapore puro. Supportata da un team di assistenza di livello mondiale, MECO offre ai propri clienti qualità, innovazione e affidabilità senza pari. Il nostro impegno per l'innovazione, la qualità e la sostenibilità ci spinge a superare continuamente i limiti della tecnologia di purificazione dell'acqua. Collaborando con MECO, le aziende farmaceutiche possono raggiungere con fiducia l'efficienza operativa e l'eccellenza del prodotto, sapendo di poter contare sul supporto di un leader di settore fidato con competenze e capacità ineguagliabili.
Collegatevi con MECO oggi stesso
Scoprite come le soluzioni di purificazione dell'acqua MECO, leader del settore, possono integrarsi perfettamente nei vostri processi produttivi, garantendo la conformità agli standard internazionali della farmacopea e guidando una crescita sostenibile. Contattate MECO oggi stesso.














