Globale Pharmakopöen-Normen und Wasserqualität für kritische Versorgungsunternehmen

Die Einhaltung strenger Pharmakopöen-Standards ist für die Gewährleistung der Produktqualität, der Sicherheit und der Einhaltung von Vorschriften in der pharmazeutischen Produktion von größter Bedeutung. Da die führenden Unternehmen in der Medikamentenentwicklung und -produktion das Tempo für die Branche vorgeben, kann die Bedeutung der Wasserqualität für wichtige Versorgungseinrichtungen bei der Einhaltung dieser Standards nicht hoch genug eingeschätzt werden.
Pharmakopöe-Normen verstehen: Eine Grundlage für die Qualitätssicherung
Pharmakopöen, die von regionalen oder nationalen Behörden erstellt werden, dienen als umfassende Sammlung von Normen und Qualitätsspezifikationen für Arzneimittel in einem bestimmten Rechtsraum. Diese Normen umfassen wichtige Parameter wie Anwendungsgebiete, Dosierungen und Qualitätskontrollmaßnahmen und bilden den rechtlichen Rahmen für die Arzneimittelherstellung.
Pharmakopöe-Spezifikationen für die Vereinigten Staaten, Europa und Asien
Ein Arzneibuch ist eine rechtsverbindliche Zusammenstellung von Normen und Qualitätsspezifikationen, die von einer regionalen oder nationalen Behörde für die in einer bestimmten Region oder einem bestimmten Land verwendeten Arzneimittel erstellt wurden. Diese Spezifikationen sind entscheidend für Anwendungsgebiete, Dosierungen und andere wichtige Faktoren, die für die behördliche Kontrolle von Arzneimitteln unerlässlich sind. Das Hauptziel der internationalen Arzneibücher ist es, einen weltweiten Standard mit einheitlichen Qualitäts- und Anwendungsspezifikationen zu schaffen.
USP-, EP- und JP-Pharmakopöe-Normen
Die Länder entwickeln nationale Pharmakopöen, um die allgemeine Gesundheit ihrer Bevölkerung durch einheitliche Standards und Spezifikationen für Arzneimittel zu unterstützen. Drei der weltweit anerkanntesten Organisationen sind die United States Pharmacopeia (USP), die European Pharmacopeia (EP) und die Japanese Pharmacopeia (JP).
Die Pharmakopöe der Vereinigten Staaten (USP): Als führende unabhängige, gemeinnützige Organisation setzt die USP weltweit den Goldstandard für Qualität, Stärke und Reinheit von Arzneimitteln. Pharmaunternehmen auf der ganzen Welt verlassen sich auf die USP-Monographien, um die Einhaltung der strengen Qualitätssicherungsparameter zu gewährleisten, die von Regulierungsbehörden wie der United States Food and Drug Administration (USFDA) durchgesetzt werden.
Europäisches Arzneibuch (EP): Das EP bietet eine umfassende Sammlung rechtsverbindlicher Monografien, die Standards für Inhaltsstoffe, Darreichungsformen und Prüfverfahren für die europäische Pharmaindustrie festlegen. Die Einhaltung der EP-Spezifikationen ist eine wesentliche Voraussetzung für den Zugang zum europäischen Markt und die Akzeptanz von Produkten.
Japanische Pharmakopöe (JP): Das JP, das auf das Jahr 1886 zurückgeht, legt Kriterien, Spezifikationen und Standardtestmethoden fest, um die Qualität und Sicherheit von Arzneimitteln in Japan zu gewährleisten. Arzneimittelhersteller auf der ganzen Welt arbeiten eng mit dem JP-Sekretariat zusammen, um die Anpassung an die neuesten wissenschaftlichen, medizinischen und technologischen Fortschritte zu gewährleisten.
Chinesische Pharmakopöe (CP): Das CP, das sich zu einem wichtigen Akteur in der globalen pharmazeutischen Landschaft entwickelt hat, legt Standards und Spezifikationen für Arzneimittel in China fest. Mit dem wachsenden Einfluss Chinas in der pharmazeutischen Industrie wird die Einhaltung der CP-Richtlinien für Unternehmen, die sich Zugang zum chinesischen Markt verschaffen und die Produktqualität sicherstellen wollen, immer wichtiger.
Pharmakopöe-Richtlinien für reines Wasser
Pharmazeutische Unternehmen verwenden pharmazeutische Wirkstoffe (APIs) zur Herstellung von Medikamenten. Diese Inhaltsstoffe sind die Elemente, die die beabsichtigte Wirkung erzielen, sei es zur Vorbeugung, Behandlung, Heilung oder Diagnose eines bestimmten Zustands oder einer Krankheit. Kombinationsarzneimittel enthalten mehr als einen Wirkstoff, der unterschiedlich wirken kann, um verschiedene Symptome zu behandeln.
Pharmakopöe-Richtlinien sind entscheidend, um sicherzustellen, dass alle Wirkstoffe unter verschiedenen Markennamen, einschließlich Generika, gleich wirken. Unternehmen, die Wirkstoffe zur Herstellung von Produkten verwenden, müssen strenge Verfahren anwenden, um eine hohe Qualität und die Einhaltung der Richtlinien zu gewährleisten. Einer der wichtigsten Bestandteile dieser Prozesse ist die Verwendung der richtigen Art von gereinigtem Wasser für eine bestimmte Herstellungsphase.
MECO beliefert pharmazeutische Unternehmen mit MASTERpak™-Systemen, die eine effiziente, einfach zu bedienende Reinigungslösung bieten. Wir entwickeln diese Systeme mit fortschrittlicher Technologie, um die Produktion von qualitativ hochwertigem Wasser zu gewährleisten, das die erforderlichen Pharmakopöe-Richtlinien erfüllt.
Wasserqualität für kritische Versorgungsunternehmen:
Sicherstellung der Einhaltung von Pharmakopöe-Normen
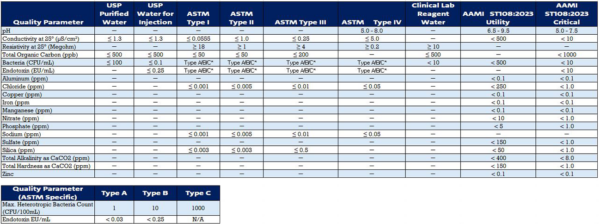
In der pharmazeutischen Produktion ist Wasser ein entscheidender Bestandteil für verschiedene Prozesse, darunter Formulierung, Reinigung und Qualitätskontrolle. Die Qualität des Wassers, das in diesen kritischen Versorgungseinrichtungen verwendet wird, einschließlich Wasser für Injektionszwecke (WFI), gereinigtes Wasser und Reinstwasser, wirkt sich direkt auf die Produktqualität und die Einhaltung der Pharmakopöenstandards aus.
 Wasser für Injektionszwecke (WFI)
Wasser für Injektionszwecke (WFI)
Wasser für Injektionszwecke ist das hochwertigste Wasser, das in der pharmazeutischen Produktion verwendet wird, und erfüllt die strengen Standards der Pharmakopöen für Reinheit und Sterilität. Es ist unverzichtbar für die Rekonstituierung von Medikamenten, die Verdünnung von Formulierungen und andere kritische Prozesse, bei denen die Reinheit des Wassers von größter Bedeutung ist.
Pharmakopöe der Vereinigten Staaten (USP):
- Leitfähigkeit:
- Nicht mehr als 1,3 µS/cm bei 25°C
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle (NaufCompendial)
- Auszählungstests: Nicht mehr als 10 KBE/100 mL
Europäisches Arzneibuch (EP):
- Leitfähigkeit:
- Nicht mehr als 1,3 µS/cm bei 20°C
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle (Nicht-Kompendium)
- Auszählungstests: Nicht mehr als 10 KBE/100 mL
Japanische Pharmakopöe (JP):
- Leitfähigkeit:
- Nicht mehr als 2,1 µS/cm
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle
- Auszählungstests: Nicht mehr als 10 KBE/100 mL
Chinesische Pharmakopöe (CP):
- Leitfähigkeit:
- Nicht mehr als 1,3 µS/cm
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle
- Auszählungstests: Nicht mehr als 10 KBE/100 mL
Diese Normen gewährleisten, dass Wasser für Injektionszwecke (WFI) die erforderlichen Reinheits- und Qualitätskriterien für die Verwendung in pharmazeutischen Herstellungsverfahren erfüllt. Pharmaunternehmen müssen sich an diese Normen halten, um die Produktintegrität zu wahren und die behördlichen Anforderungen in ihren jeweiligen Regionen zu erfüllen.
Gereinigtes Wasser (PW)
Gereinigtes Wasser entspricht den Spezifikationen der Pharmakopöe für chemische und mikrobiologische Reinheit und wird in verschiedenen pharmazeutischen Prozessen wie Formulierung, Reinigung und Labortests verwendet. Es ist von entscheidender Bedeutung für die Wahrung der Produktintegrität und die Einhaltung der gesetzlichen Vorschriften.
Pharmakopöe der Vereinigten Staaten (USP):
- Leitfähigkeit:
- Nicht mehr als 1,3 µS/cm bei 25°C
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle
- Auszählungstests: Nicht mehr als 100 KBE/ml
Europäisches Arzneibuch (EP):
- Leitfähigkeit:
- Nicht mehr als 5,1 µS/cm bei 20°C
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle
- Auszählungstests: Nicht mehr als 100 KBE/ml
Japanische Pharmakopöe (JP):
- Leitfähigkeit:
- Nicht mehr als 4,3 µS/cm bei 25°C
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle
- Auszählungstests: Nicht mehr als 100 KBE/ml
Chinesische Pharmakopöe (CP):
- Leitfähigkeit:
- Nicht mehr als 5,1 µS/cm bei 25°C
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle
- Auszählungstests: Nicht mehr als 100 KBE/ml
Diese Normen gewährleisten, dass gereinigtes Wasser die erforderlichen Reinheits- und Qualitätskriterien für pharmazeutische Herstellungsverfahren erfüllt. Die Einhaltung dieser Normen ist für Pharmaunternehmen unerlässlich, um die Produktintegrität zu wahren und die behördlichen Anforderungen in ihren jeweiligen Regionen zu erfüllen.
Ultrareines Wasser (UPW)
Ultrapure Water übertrifft die Standards der Pharmakopöe für die Wasserreinheit und wird in sensiblen pharmazeutischen Anwendungen wie Chromatographie, Molekularbiologie und analytischen Tests eingesetzt. Sein ultrahoher Reinheitsgrad gewährleistet Genauigkeit und Zuverlässigkeit bei kritischen Laborverfahren.
Pharmakopöe der Vereinigten Staaten (USP):
- Leitfähigkeit:
- Nicht mehr als 1,3 µS/cm bei 25°C
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle
- Auszählungstests: Nicht mehr als 100 KBE/ml
Europäisches Arzneibuch (EP):
- Leitfähigkeit:
- Nicht mehr als 0,1 µS/cm bei 25°C
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle
- Auszählungstests: Nicht mehr als 10 KBE/ml
Japanische Pharmakopöe (JP):
- Leitfähigkeit:
- Nicht mehr als 0,1 µS/cm bei 25°C
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle
- Auszählungstests: Nicht mehr als 100 KBE/ml
Chinesische Pharmakopöe (CP):
- Leitfähigkeit:
- Nicht mehr als 0,1 µS/cm bei 25°C
- Insgesamt
- Organischer Kohlenstoff (TOC): Nicht mehr als 500 ppb
- Bakterielle
- Endotoxine: Nicht mehr als 0,25 EU/ml
- Mikrobielle
- Auszählungstests: Nicht mehr als 100 KBE/ml
Diese Normen stellen sicher, dass Ultrapure Water die strengen Qualitätsanforderungen der Pharmakopöen erfüllt und somit für den Einsatz in sensiblen pharmazeutischen Anwendungen, analytischen Tests und in der Forschung geeignet ist. Pharmazeutische Unternehmen müssen diese Standards einhalten, um die Produktintegrität zu wahren und die behördlichen Anforderungen in ihren jeweiligen Regionen zu erfüllen.
Partnerschaft mit MECO für umfassende Wasserreinigungslösungen
Bei MECO ist unser umfassender Ansatz für Wasserreinigungslösungen speziell auf Biotechnologie-, Pharma- und Biowissenschaftsunternehmen sowie auf Forschung und Entwicklung zugeschnitten. Wir entwickeln und produzieren alle erforderlichen Technologien zur Herstellung von Water for Injection (WFI), gereinigtem Wasser, Reinstwasser und Reinstdampf und stellen damit sicher, dass unsere Kunden Zugang zu einem umfassenden Angebot an branchenführenden Wasserreinigungslösungen haben.
Innovation und Exzellenz vorantreiben
Mit fast einem Jahrhundert Erfahrung in der Wasserindustrie hat sich MECO als führender Anbieter von Wasseraufbereitungslösungen etabliert. Seit 1928 bieten wir hochmoderne Systeme an, die den strengen Anforderungen der Pharmakopöe entsprechen.
MECO ist stolz auf seine Produktionsstätten in Mandeville, LA, und San Diego, CA (Water Works), wo wir alle notwendigen Technologien zur Herstellung von Water for Injection (WFI), Purified Water (PW), Ultrapure Water (UPW) und Reinstdampf entwickeln und herstellen. MECO wird von einem erstklassigen Serviceteam unterstützt und bietet seinen Kunden unübertroffene Qualität, Innovation und Zuverlässigkeit. Unser Engagement für Innovation, Qualität und Nachhaltigkeit treibt uns an, die Grenzen der Wasseraufbereitungstechnologie ständig zu erweitern. Durch die Zusammenarbeit mit MECO können Pharmahersteller ihre betriebliche Effizienz und Produktqualität steigern, denn sie wissen, dass sie von einem vertrauenswürdigen Branchenführer mit unübertroffenem Fachwissen und Fähigkeiten unterstützt werden.
Heute mit MECO in Verbindung treten
Entdecken Sie, wie MECOs branchenführende Wasseraufbereitungslösungen nahtlos in Ihre Produktionsprozesse integriert werden können, um die Einhaltung der internationalen Pharmakopöenstandards zu gewährleisten und nachhaltiges Wachstum zu fördern. Kontaktieren Sie MECO noch heute.














